Drobnoustroje to przebiegłe organizmy wykazujące zadziwiające cechy. Przez tysiące lat tak ewoluowały, że wykształciły zdolność do oporności na stosowanie środków przeciwdrobnoustrojowych (AMR). Coraz częściej mówi się o tym, że antybiotyki są nieskuteczne i terapie zawodzą. Z powodu AMR corocznie na świecie umiera ok. 1,3 mln ludzi, a prognozy sugerują, że w 2050 r. takich przypadków będzie 10 mln. Poza cierpieniem ludzkim ma to też wymiar finansowy – Bank Światowy przewiduje, że z powodu AMR globalny PKB będzie mniejszy o 3,4 bln dol. rocznie w perspektywie do 2030 r.
Wraz z poprawiającym się dobrostanem społeczeństw na świecie i wydłużającym się oczekiwanym czasem życia coraz istotniejsza staje się koncentracja na rozwiązaniu problemu oporności na środki przeciwdrobnoustrojowe. Kategoria obejmuje antybiotyki, leki przeciwwirusowe, leki przeciwgrzybiczne i środki przeciwpierwotniakowe, w których substancja czynna jest pochodzenia syntetycznego lub naturalnego. AMR to zdolność mikroorganizmów do zwiększania swojej oporności na środek przeciwdrobnoustrojowy, na który były wcześniej wrażliwe.
Innymi słowy, przykładowo bakterie są zdolne bronić się przed antybiotykami za pomocą różnych mechanizmów, a gdy stają się oporne to potrafią się namnażać w obecności leku i mogą przekazywać zdolność obrony kolejnym pokoleniom. Niejednokrotnie zdarza się w czasie terapii, że okazuje się ona nieskuteczna i zachodzi potrzeba sięgnięcia po inny antybiotyk. Jeszcze gorzej, jeżeli wiele antybiotyków nie działa odpowiednio, gdyż poza wątpliwym skutkiem terapeutycznym ich stosowanie ma także skutki uboczne. I to jest poważne wyzwanie globalne, z którym mierzy się cały świat. Tym bardziej poważne, że dotyczy szerokiego spektrum świata żywego – ludzi, zwierząt i roślin.
Sprawa nie jest nowa. Jest znana od lat i to wielu. Na zagrożenie wskazywał Alexander Fleming, odkrywca penicyliny, który podczas odbierania Nagrody Nobla w 1945 r. ostrzegał, że mikroby są w stanie przyspieszyć rozwój oporności pod wpływem zwiększonej presji selekcyjnej wynikającej z powszechnego stosowania antybiotyków i innych środków przeciwdrobnoustrojowych.
WHO alarmuje
Na początku grudnia WHO opublikowała raport Global Antimicrobial Resistance and Use Surveillance System (GLASS) na temat AMR – z jego pełną treścią zapoznasz się TUTAJ.
Opracowanie dowodzi m. in., że wysoki poziom (powyżej 50%) oporności odnotowano u bakterii często powodujących zakażenia krwi w szpitalach, takich jak Klebsiella pneumoniae i Acinetobacter spp. Ponad 60% izolatów Neisseria gonorrhoea, powszechnej choroby przenoszonej drogą płciową, cechuje oporność na jeden z najczęściej stosowanych doustnych środków przeciwbakteryjnych – ciprofloksacynę. A przeszło 20% izolatów E.coli – najczęstszego patogenu w zakażeniach dróg moczowych – było odpornych zarówno na leki pierwszego rzutu (ampicylina i kotrimoksazol), jak i na leki drugiego rzutu (fluorochinolony).
Organizacja przyznała, że choć większość trendów w zakresie oporności była stabilna w ciągu ostatnich czterech lat, to zakażenia krwi z powodu opornych Escherichia coli i Salmonella spp. oraz oporne zakażenia rzeżączką wzrosły o co najmniej 15% w porównaniu do poziomu z 2017 r. To jednak jedynie wycinek zagadnienia.
Czy czekają nas ciemne wieki w medycynie z powodu AMR?
The Lancet w tym roku opublikował artykuł, z którego wynika, że liczba śmierci spowodowanych przez AMR w 2019 r. wyniosła 1,27 mln (12. przyczyna zgonów według danych WHO), czyli więcej niż w przypadku HIV/AIDS (864 tys. zgonów), raka piersi (701 tys.) czy malarii (643 tys.). Dane te są z pewnością niedoszacowane, ponieważ brakuje danych z wielu krajów o niskich i średnich dochodach – analizę przeczytasz TUTAJ.
Wydawałoby się, że liczba zgonów z powodu oporności na środki przeciwdrobnoustrojowe jest niewielka, jeżeli porówna się z ośmiomiliardową populacją naszej planety. Istnieje jednak obawa, iż do 2050 r. AMR może powodować większą liczbę zgonów niż choroba nowotworowa.
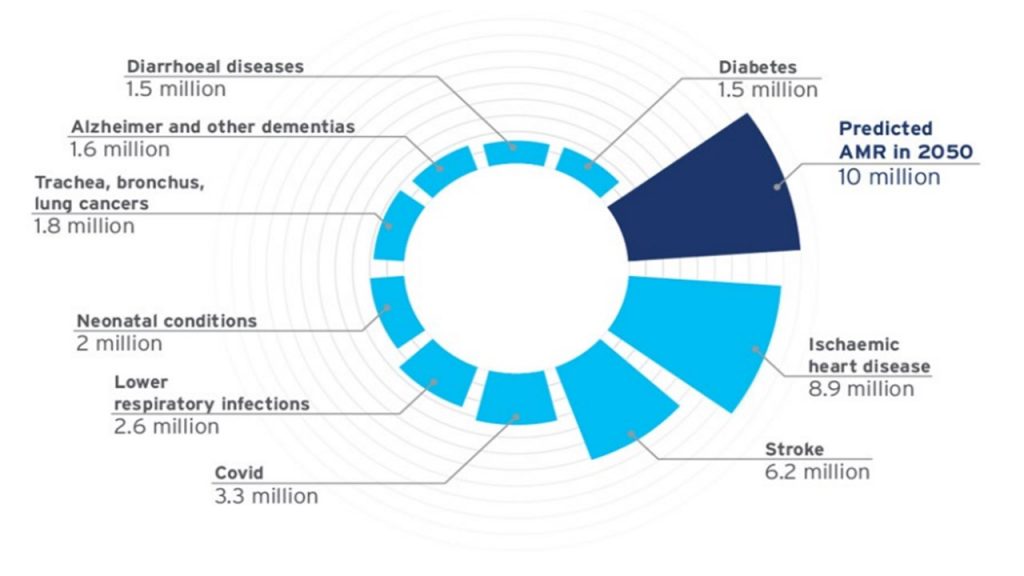
Zdaniem ekspertów oporność na środki przeciwdrobnoustrojowe będzie pogłębiać się, co odbije się na dobrostanie ludzkim w dwóch wymiarach. UN Ad hoc Interagency Coordinating Group ds. AMR przewiduje, że do 2050 r. liczba zgonów związanych z opornością osiągnie 10 mln rocznie na całym świecie. Bank Światowy z kolei prognozuje, że do 2030 r. uszczerbek na globalnym PKB z powodu AMR wyniesie 3,4 bln dol. rocznie – dla porównania instytucja podała, że światowy PKB w 2021 r. zamknął się kwotą ok. 96 bln dol. Żeby sobie uświadomić, jaka jest to skala zagrożenia, warto odwołać się do danych na temat pandemii koronawirusa, która wstrząsnęła kulą ziemską, zwłaszcza w 2020 r.
„[…] świat przeszedł przez pandemię COVID-19, w której zginęły miliony ludzi, a spadek globalnego PKB wyniósł blisko 8 bln dol.” – powiedział Lord O’Neill of Gatley, członek Izby Lordów brytyjskiego parlamentu przez wiele lat związany z bankiem inwestycyjnym Goldman Sachs (m. in. główny ekonomista).
Nieco inne szacunki niż Bank Światowy zaprezentował Review on Antimicrobial Resistance (RAR) – treść badania znajduje się TUTAJ.
Ta wspierana przez rząd brytyjski inicjatywa doszła do wniosku, że jeżeli świat nie stawi czoła AMR, to koszt w postaci utraconej produkcji światowej w latach 2016-2050 wyniesie 100 bln dol.
„Jeśli nie podejmiemy działań, czeka nas niemal nie do pomyślenia scenariusz, w którym antybiotyki przestaną działać i zostaniemy z powrotem wrzuceni w ciemne wieki medycyny” – skomentował wnioski RAR David Cameron, były premier Wielkiej Brytanii.
Niekończąca się walka trwa
Walka z drobnoustrojami wydaje się zadaniem nigdy się nie kończącym. Naukowcy opracowują nowe środki, licząc się z tym, że w końcu wystąpi zjawisko oporności na nie. Dotyczy to m. in. antybiotyków. W skrajnych sytuacjach bywa tak, że niekiedy już na etapie badań klinicznych, a zatem jeszcze przed wprowadzeniem środka do powszechnej terapii, badacze identyfikują zjawisko oporności w niektórych kategoriach drobnoustrojów. Często chodzi też o to, że już w niezwykle krótkim czasie po wprowadzeniu środka do stosowania zaobserwować można AMR.
Co szczególnie niepokojące, dochodzi do tego przede wszystkim w ostatnich dekadach – mniej więcej od lat 70. W niektórych kategoriach oporność występowała po maksymalnie kilku latach od wprowadzenia do praktyki leczniczej – czasami dawało się to policzyć na palcach jednej dłoni. To przypadek m. in. ketolidów, glicylocyklin, monobaktam, oksazolidynon czy karbapenem. Wcześniej niektóre środki przeciwdrobnoustrojowe przeciwstawiały się mikroorganizmom przez o wiele dłuższy czas (zwykle kilkanaście lat). Dobrze ten niepożądany trend obrazuje poniższa infografika, gdzie skrót D oznacza „odkrycie cząsteczki”, CI „zatwierdzenie środka przez organ nadzorczy, a następnie wprowadzenie do powszechnej terapii”, zaś RF „odkrycie oporności”.

Wyzwania w związku z AMR
Czynników odpowiedzialnych za oporność na środki przeciwdrobnoustrojowe jest sporo. Bez szczególnego niuansowania można je podzielić na trzy grupy:
– nadużywanie i niewłaściwe stosowanie środków w działaniach ukierunkowanych m. in. na ludzi i zwierzęta (w tym terapiach),
– niedostateczna higiena i warunki sanitarne,
– oraz deficyt badań i innowacji, mających na celu wynalezienie nowych środków przeciwdrobnoustrojowych.
Zacznijmy od pierwszego czynnika. Środek przeciwdrobnoustrojowy to z pewnością nie jest suplement diety, z którym też zresztą można przeholować. Sporo ludzi wykazuje z różnych przyczyn inklinację do samoleczenia, a internet i pokątny handel stacjonarny sprzyja tego typu zachowaniu. Problem z tym podejściem jest taki, że wiedza olbrzymiej większości samoleczących się jest dalece niewystarczająca, aby podjąć się trudu terapii. Skutki takiego ryzykownego zachowania mogą być w najlepszym razie opłakane, a w najgorszym tragiczne.
Komisja Europejska (KE) podała w listopadzie, że mieszkańcy Wspólnoty przyjmowali ok. 8% antybiotyków bez recepty. Można przypuszczać, że wielu z nich nie stawiło się na konsultacje lekarskie, a zatem szukało rozwiązania w postaci samoleczenia. To i tak nie jest fatalny rezultat, ponieważ w niektórych miejscach stosowanie na własną rękę leków przeciwdrobnoustrojowych, w tym antybiotyków, odbywa się na o wiele większą skalę. Archives of Public Health opublikowało w 2021 r. badanie na temat używania antybiotyków w wybranych krajach o średnim i niskim dochodzie (m. in. Indie, Pakistan, Nepal, Nigeria i Gwatemala). Częstość występowania samoleczenia wahała się w przedziale 50,0-93,8%, a łączna częstość wyniosła 78%. Pełne opracowanie znajdziesz TUTAJ.
Kolejnym problemem jest zjawisko nadużywania środków przeciwdrobnoustrojowych. I znowu można odnieść się do antybiotyków, ponieważ ta kategoria wydaje się najlepiej zbadana, choć i tak jest to wciąż wiedza fragmentaryczna. Journal of the American Medical Association podał, że ok. 30% antybiotyków w Stanach Zjednoczonych było niepotrzebnie przepisywanych przez lekarzy. Mogło być parę przyczyn tego stanu rzeczy – na przykład być może kłopotliwa okazywała się diagnoza stanu zdrowia, a być może było to efektem presji na zaordynowanie leku, którą wywoływał pacjent. Jeszcze gorsze wyniki mogą cechować gospodarki mniej rozwinięte. Jedno z badań zamieszczonych w BMJ Global Health wskazało, że niewłaściwe przepisywanie antybiotyków dotyczyło ok. 50% pacjentów z Indii i Kenii.
A jak to wygląda w Polsce? Niewykluczone, że najlepszy ogląd sytuacji daje raport NIK z 2019 r., w którym opisana została konsumpcja środków przeciwbakteryjnych (dane za 2017 r.). Izba wskazała, że spożycie tych preparatów w lecznictwie otwartym (pozaszpitalnym) było powyżej średniej europejskiej Dawki Dobowej Definiowanej (DDD) – w naszym kraju było to 27 DDD na 1 tys. mieszkańców. Średnia dla obszaru UE/EOG wyniosła 21,8 DDD przy rozpiętości od 10,1 DDD (Holandia) do 33,6 DDD (Cypr). Z treścią informacji o wynikach kontroli zapoznasz się TUTAJ.
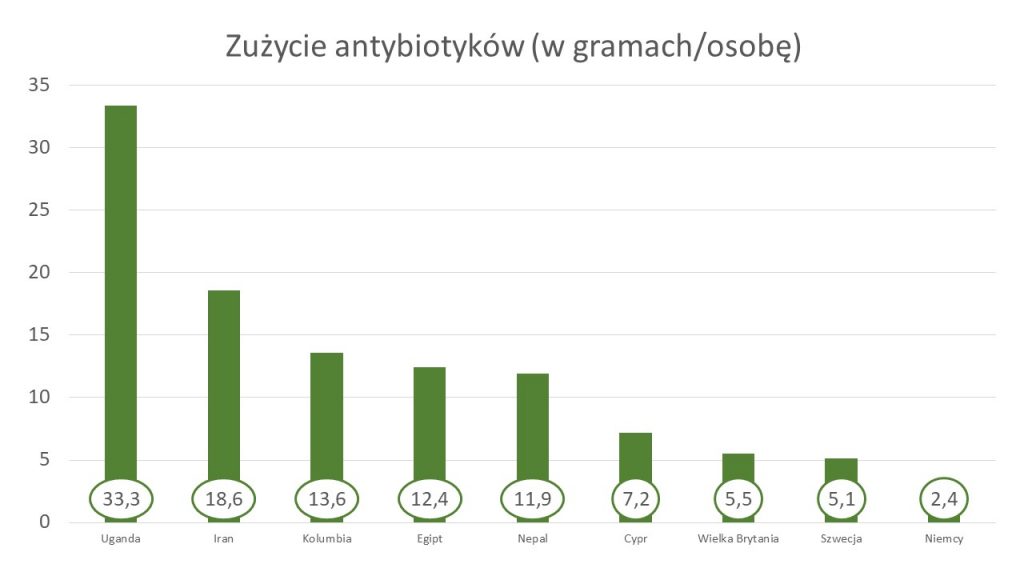
Tegoroczny raport GLASS uprawdopodabnia występowanie rozdźwięku między państwami rozwiniętymi a pozostałymi (nie ma w nim danych dla Polski). W tych pierwszych zjawisko nadużywania antybiotyków wydaje się, że nie jest rozpowszechnione. W wybranych gospodarkach europejskich zużycie antybiotyków na osobę rocznie nie przekraczało 10 gramów. Znacznie większa konsumpcja charakteryzowała państwa mniej zamożne.
„W krajach o niskich i średnich dochodach oporność jest już wysoka i przewiduje się, że AMR będzie rósł szybciej niż w krajach OECD. Na przykład w Indonezji, Brazylii i Rosji od 40% do 60% zakażeń jest już opornych w porównaniu ze średnią 17% w krajach OECD. Przewiduje się, że w tych krajach wzrost wskaźników oporności na środki przeciwdrobnoustrojowe będzie od 4 do 7 razy szybszy niż w krajach OECD w latach 2018-2030. Tak wysokie wskaźniki oporności w systemach opieki zdrowotnej, które już teraz są osłabione przez ograniczone budżety, stworzą warunki do ogromnej śmiertelności, która będzie dotyczyć głównie noworodków, bardzo małych dzieci i osób starszych” – ostrzega OECD.
„Skuteczne antybiotyki mają kluczowe znaczenie dla współczesnej medycyny. Na przykład pacjenci poddawani chemioterapii lub przeszczepom polegają na antybiotykach, aby uniknąć infekcji i powikłań. Jednak rosnąca oporność na środki przeciwdrobnoustrojowe po pół wieku nadmiernego przepisywania antybiotyków budzi obawy, że szpitalom zabraknie możliwości ratowania życia […]” – czytamy w raporcie organizacji, którego całość znajdziesz TUTAJ.
Za większość zużycia środków przeciwdrobnoustrojowych odpowiadają zwierzęta (ok. 70-80%). Intensyfikacja rolnictwa prowadzi do tego, że będzie ono rosło (o 2/3 do 2030 r.), co najbardziej ma dotknąć gospodarki wschodzące (Brazylia, Rosja, Indie, Chiny i RPA). Istotna część konsumpcji nie idzie wcale na leczenie infekcji. Służy ona bowiem do maksymalizacji wydajności przemysłu rolniczego poprzez zwiększenie wzrostu zwierząt i umożliwienie trzymania ich na mniejszych powierzchniach, a tym samym w mniej sanitarnych warunkach, przy zmniejszonym ryzyku zachorowania. Przykładów takiego postępowania nie brakuje. W regionie delty Mekongu 84% zużycia antybiotyków w celach hodowlanych miało na celu profilaktykę – kłania się tutaj słynna panga. Wspieranie wzrostu zwierząt odpowiadało za 53% konsumpcję środków przeciwdrobnoustrojowych w Chinach.
Rozwojowi AMR sprzyja również niedostateczna higiena i warunki sanitarne. Chodzi tutaj m. in. o przenoszenie opornych patogenów ze zwierząt na ludzi, uwalnianie substancji przeciwdrobnoustrojowych do środowiska, które ostatecznie trafiają do wód gruntowych. W to wpisują się też zmiany klimatyczne, w wyniku których zwiększa się częstotliwość i intensywność ekstremalnych zjawisk (np. powodzie), co utrudnia zachowanie właściwych warunków sanitarnych.
„Za każdym razem, gdy […] następuje powódź, jak na przykład podczas ostatnich tragicznych wydarzeń w Pakistanie, nie tylko cholera i szigeloza stanowią problem, ale dochodzi do niewyobrażalnego rozprzestrzenienia się bakterii AMR ze zwierzęcych i ludzkich odchodów, a w efekcie zanieczyszczenia wody pitnej w wielu społecznościach” – uważa prof. Timothy R. Walsh, OBE Director of Biology z Ineos Oxford Institute for Antimicrobial Research.
Niedoinwestowanie AMR jest faktem
Odpowiedzią na wyzwania związane z AMR mogłyby być nowe odkrycia. A z tym jest po prostu krucho. Większość międzynarodowych projektów zakończyła działalność w tej dziedzinie, a na placu boju w zasadzie pozostały jedynie GSK i Pfizer, które należą do nielicznych dużych firm zaangażowanych w programy badawcze.
W 2019 r. tylko 6 z 32 antybiotyków w fazie badań klinicznych, które dotyczyły priorytetowych patogenów z listy WHO, można było uznać za innowacyjne. Firmy farmaceutyczne nie kwapią się, aby ponosić znaczne nakłady inwestycyjne na badania i rozwój. Bo im się to zwyczajnie może nie opłacać. Office for Health Economics oszacował, że wartość bieżąca netto nowego antybiotyku wynosi 50 mln dol., co znacząco odbiega od ok. 1 mld. dol. w przypadku cząsteczki stosowanej w leczeniu chorób nerwowo-mięśniowych.
Podobnie ostrożnie zachowują się dawcy kapitału. W latach 2003-2013 na 38 mld dol. zainwestowanych przez venture capital (kapitał podwyższonego ryzyka) w farmację tylko 1,8 mld dol. zasiliło projekty ukierunkowane na badania nad środkami przeciwdrobnoustrojowymi. Niezbyt chętne inwestycjom w ten segment bywają również agendy rządowe. Przykładowo amerykański Narodowy Instytut Zdrowia (NIH) przeznaczył w latach 2009-2014 zaledwie 1,2% funduszy grantowych na badania związane z AMR – dla porównania na terapie związane z rakiem współczynnik wyniósł ponad 18%.
Sektor farmaceutyczny stanął w obliczu paradoksu. Z jednej strony w debacie publicznej AMR jawi się coraz bardziej jako palący problem do rozwiązania, który jeżeli nic nie zrobimy może wymknąć się spod kontroli. Powoli przestaje on być domeną kręgów akademickich, które wskazują coraz powszechniej na zagrożenia. Literatura fachowa poświęcona oporności na środki przeciwdrobnoustrojowe wzrosła w latach 1990-2018 wykładniczo – z 2 tys. artykułów (1990) do ponad 11 tys. pozycji (2018). Z drugiej jednak strony słychać nawoływanie do ograniczenia spożycia antybiotyków, które powinny być formą terapii, gdy inne metody zawiodą. A to oznacza naturalne ryzyko ograniczenia popytu na tę klasę leków. Co z kolei przełożyłoby się na mniejszą sprzedaż koncernów farmaceutycznych i mogłoby wiązać się z niewystarczającą opłacalnością projektów inwestycyjnych.
Aby wybrnąć z tego impasu coraz częściej w państwach rozwiniętych dyskutuje się nad wdrożeniem modelu subskrypcji à la Netflix. Polegałoby to na tym, że rządy wnosiłyby roczną opłatę abonamentową na rzecz firm farmaceutycznych w zamian za dostęp do portfela innowacyjnych produktów, a nie płaciłyby w zależności od przepisanej liczby leków.
„Przede wszystkim rządy powinny wprowadzić zachęty ekonomiczne oraz podejście do refundacji, które stymuluje inwestycje i innowacje w zakresie antybiotyków poprzez zapewnienie zwrotu kosztów dla innowatorów przy jednoczesnym utrzymaniu idealnie niskich ilości przepisywanych leków” – zauważyła Emma Walmsley, prezes zarządu GSK.
„Widzieliśmy już tego przykład w działaniu – w postaci pilotażowego modelu płatności abonamentowych za antybiotyki, realizowanego przez rząd Wielkiej Brytanii. Próba pokazała, że możliwe jest zaprojektowanie i wdrożenie bodźców przyciągających, gdzie płaci się za wartość, a nie za ilość” – dodała.
Innym rozwiązaniem, które rozważa KE, jest koncepcja Transferable Exclusivity Extension (TEE). TEE byłoby programem zachęt dla Big Pharmy, który zakładałby, że w zamian za opracowanie nowego środka przeciwinfekcyjnego koncern dostawałby wydłużoną ochronę patentową na terenie UE na inny swój lek. Jak nie trudno zgadnąć, koncepcja spotkała się z krytyką ze strony rządów i konsumentów, które były zdania, że przyczyni się to do znacznego wzrostu wydatków na ochronę zdrowia.
Katarzyna Kosiorek, analityczka Trigon DM, zajmująca się spółkami z obszaru life sciences

Choć zjawisko antybiotykoodporności mikroorganizmów jest znane od dawien dawna w nauce, to w ostatnich latach nabiera charakteru rozpędzonej lawiny i w literaturze fachowej często określane jest mianem „cichej pandemii”. Tak jak to zostało już wcześniej przytoczone, rocznie z powodu AMR umiera więcej pacjentów niż z powodu HIV/AIDS czy malarii. Według Światowej Organizacji Zdrowia oporność na środki przeciwdrobnoustrojowe jest jednym z dziesięciu największych zagrożeń dla zdrowia publicznego na świecie. Według AMR Action Fund superbakterie – bakterie odporne na leki – mogą każdego roku zabijać miliony ludzi, a szkody dla zdrowia potencjalnie mogą przewyższyć szkody humanitarne i finansowe spowodowane przez COVID-19. Co możemy zrobić aby ograniczyć zjawisko AMR? Jeśli mamy kontrolować oporność na antybiotyki, musimy myśleć o terapii przeciwdrobnoustrojowej w nowy sposób.
Można unieszkodliwić, zamiast zabijać. Jedną z metod jest selektywne zwalczanie bakterii chorobotwórczych, bez ich zabijania. Większość bakterii nie musi wywoływać choroby, aby przetrwać, więc jeśli nasze terapie nie mają na celu ich zabicia, selekcja odpornych mutantów będzie słaba – co oznacza, że mogą one nadal żyć, nie wyrządzając nam krzywdy.
Można celować w nowe mechanizmy wirulencji. Alternatywnie, moglibyśmy terapeutykami celować w geny, których bakterie potrzebują do wywołania choroby, czyniąc je nieszkodliwymi bez zakłócania wzrostu bakterii. To podejście również umożliwiłoby zmniejszenie ilości używanych antybiotyków. Można przyspieszyć proces odkrywania nowych leków z pomocą sztucznej inteligencji i komputerów kwantowych. Świat może znaleźć nowe leki, z którymi bakterie jeszcze się nie spotkały lub których pokonanie będzie trudne. „Generatywne” modele sztucznej inteligencji tworzą hipotezy dotyczące ostatecznej cząsteczki potrzebnej do powstania konkretnego nowego leku. Modele te nie tylko wyszukują znane cząsteczki o odpowiednich właściwościach, ale są wystarczająco silne, aby poznać cechy danych leżących u ich podstaw i mogą sugerować nowe cząsteczki, które nie zostały jeszcze zsyntetyzowane.
Ale… trzeba współpracować i zwiększać świadomość społeczną. Najważniejszym elementem pozostaje zapewnienie ściślejszej współpracy wszystkich podmiotów w walce z opornością na środki przeciwdrobnoustrojowe, a także krytycznego uwzględnienia lekooporności w inicjatywach na rzecz bezpieczeństwa zdrowotnego. Współpracując w wielu sektorach (m.in. farmaceutycznym, rolniczym, spożywczym) możemy powstrzymać kolejne duże globalne zagrożenie dla zdrowia, w tym oporności na środki przeciwdrobnoustrojowe.






